中国癌症死亡人数占全球的四分之一 癌症的精准治疗有可能吗?


独家抢先看
每五个人,就有一个会患癌症而每七个人,就会最终死于癌症穿刺检测,让癌症检测痛苦不堪用一管血液实现癌症的精准检测使癌症的精准治疗成为可能。
和【CC讲坛演讲】一起,来听北京大学生命科学院研究员白凡,讲述未来的癌症检测,如何才能不痛苦,以及癌症的个性化治疗,如何实现。
每七个人里,就会有一个人最终死于癌症
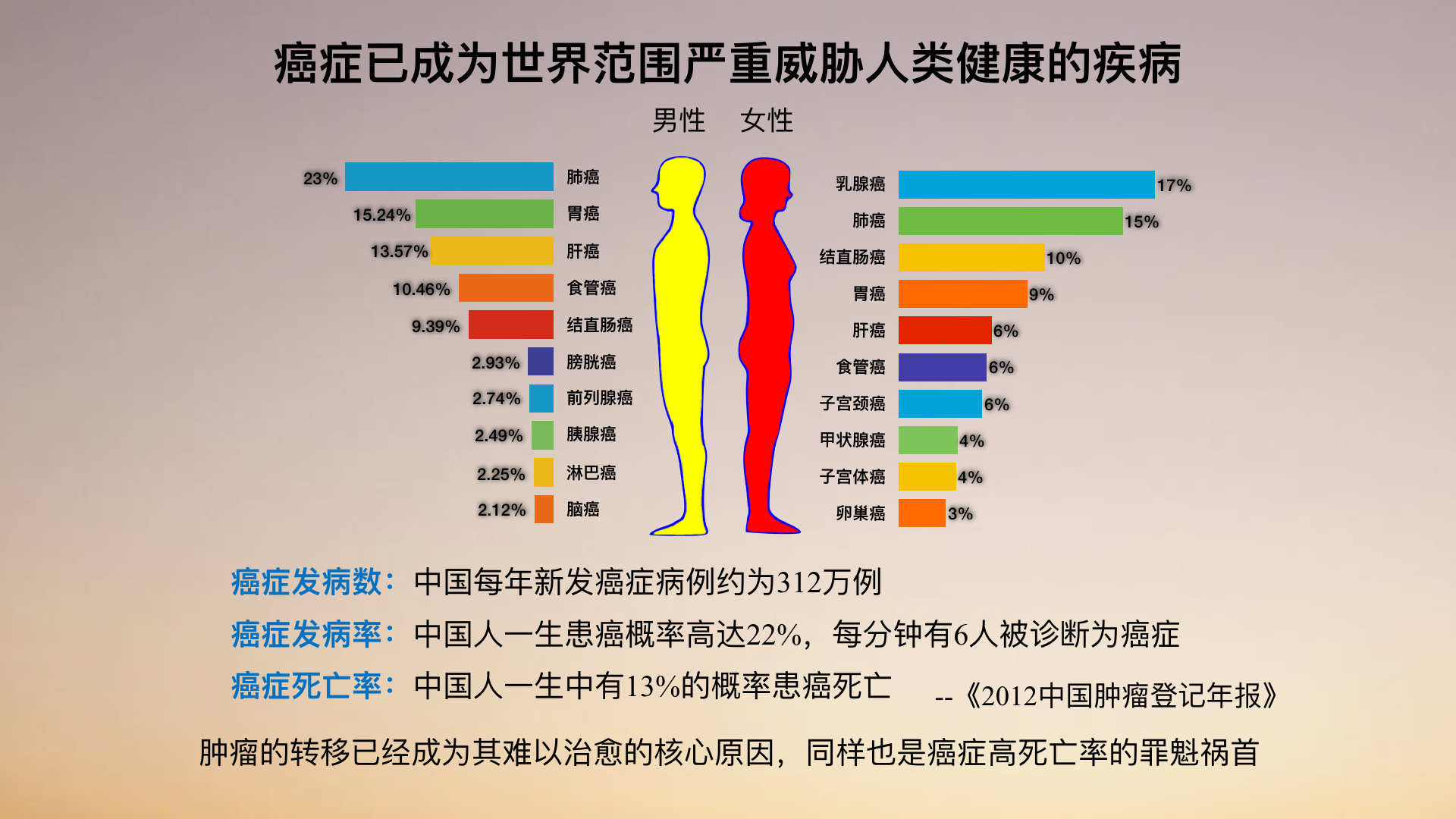
我今年35岁。在过去的一年之内,我在北京大学读书时候的同学里面有两位因为癌症离开了这个世界。我想这样不幸的故事也在在座的各位周围发生过。癌症已经成为全世界严重威胁人类健康的疾病。在我们中国也是这样,平均每五个人里面就有一个人在一生的时间之内会患癌症,每七个人里面会有一个人在一生的时间之内最终死于癌症。这个数据还在不断地上升。
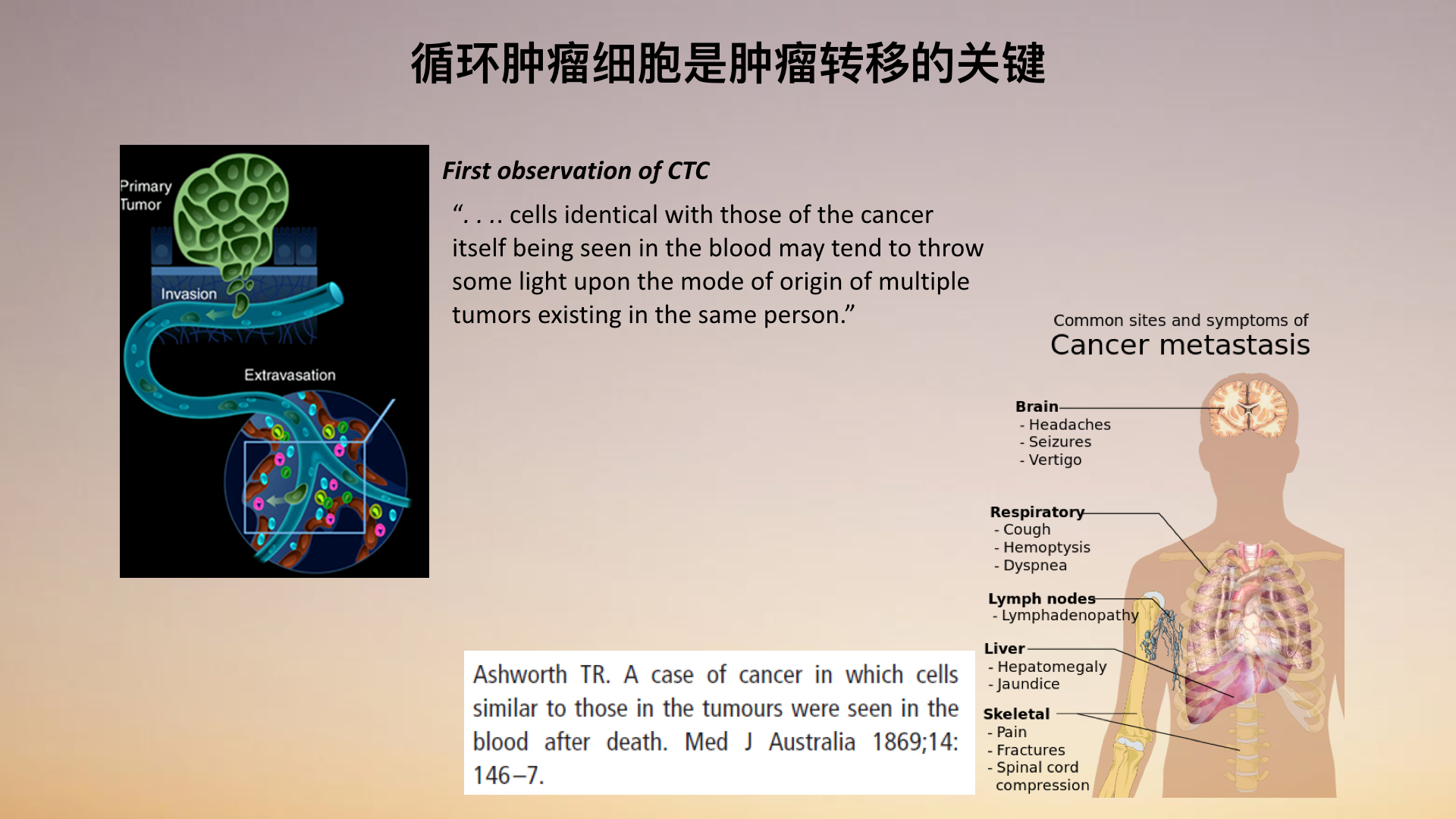
尽管我们今天已经有了非常先进的医学的检测手段、手术的技术、还有药物的技术,我们依然没有办法去治疗癌症。其主要的原因就是因为癌症它和别的疾病不太一样,癌症具有广泛的多器官的转移。癌症的转移主要是通过血液循环系统来进行的。在癌症病人的血液里面存在着这样一些循环的肿瘤细胞。
它们就像种子一样在病人的血液里面循环着游荡着,然后去找寻适合它们生存的土壤,而一旦它们找到了这样的土壤就会去播散更多地转移。
经过一个多世纪的研究,我们现在对于癌症的转移已经有了比较清晰的认识。
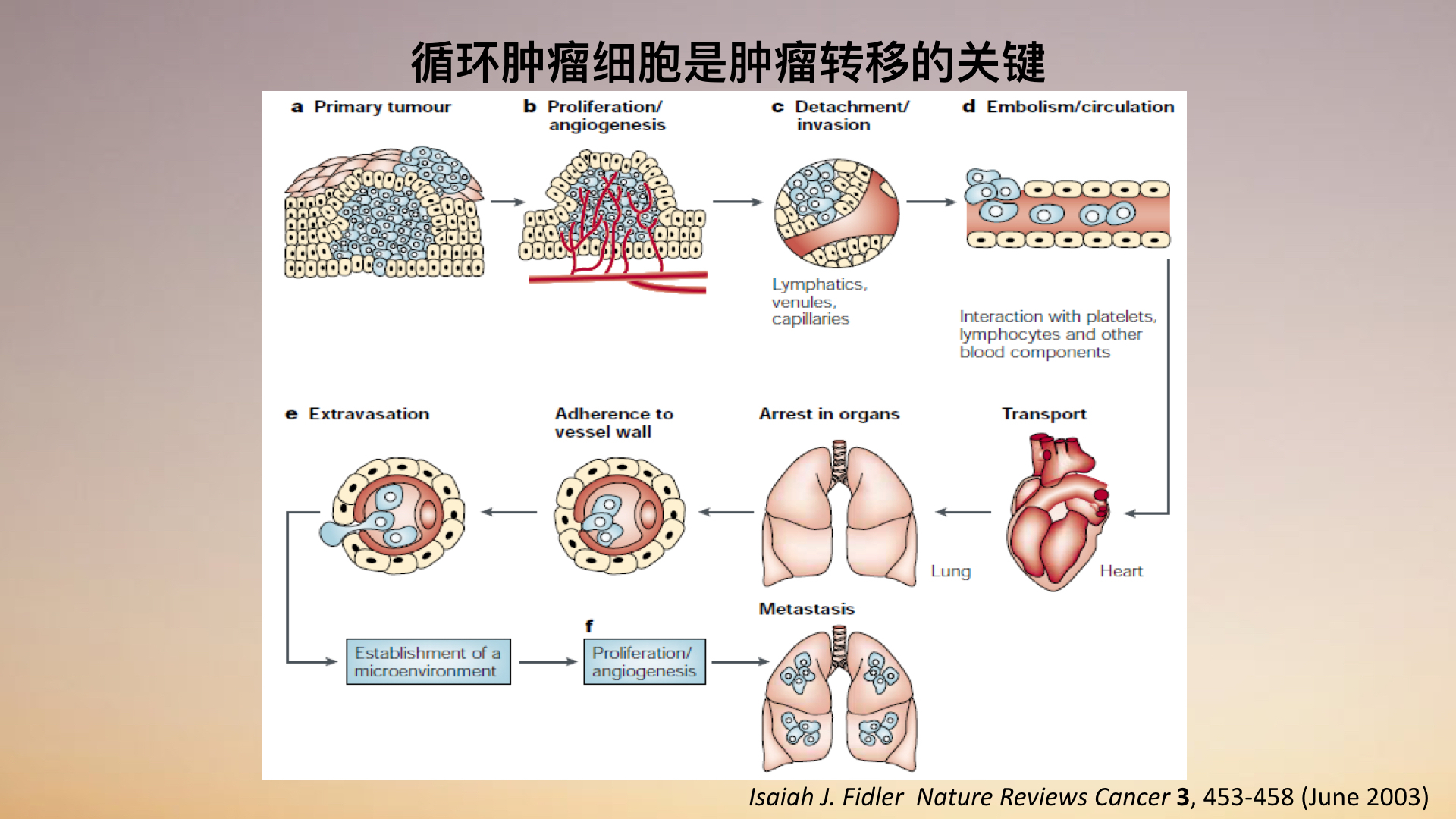
癌症转移,究竟有几个步骤?
首先大家看一下这幅图。这幅图上总结了癌症转移的几个主要的步骤。首先,在人体里面,每天我们的细胞都会经历很多的外界的刺激,会发生不断地去复制,去分裂,这些过程中会引入一些新的基因突变。这样一些基因突变的产生会让这些细胞获得特异的特性。它们摆脱了细胞跟细胞之间生长上的抑制,以及繁殖代数的限制,它们就会疯狂地生长起来。这些就形成了原位的肿瘤。
而原位的肿瘤在长大的过程中会分泌出很多细胞的因子,这些细胞因子会吸引可以形成血管的内皮细胞向肿瘤靠拢。这些血管一旦和肿瘤交互生长在了一起就给肿瘤的生长提供了更多的养分和氧气。与此同时,也给予肿瘤进入血管提供了一个机会。其中有一些比较厉害的肿瘤细胞,它们具有更强的迁移和这种爬行的能力,能够穿出原来的位置然后进入到血管。一旦它们进入到血管,就好像一个歹徒,一个罪犯开着车上了高速公路。我们再想抓住它们就很难了。这些进入血管的肿瘤细胞随着我们身体的循环系统就会快速地播散到我们的其它器官。
而一旦它们在其它器官的这些毛细血管里面再一次停留下来,它们就会启动另外的生物学过程,再一次地穿出血管,然后建立起一个转移灶。
这就是肿瘤转移的几个主要的步骤。这些步骤在我们生物学的实验室里面已经得到了很好的研究,在医学的临床上也得到了很好的研究。只是其中这个作为肿瘤转移这个最关键的媒介也就是病人血液里面的循环肿瘤细胞的研究一直非常的有限,其主要原因就在于技术手段的限制。
我这里给大家展示的是一管我们人类的血,有三毫升。
大家可以把自己想象成为一个小小的机器人,到这个血液里面去看一下它的微观的环境,就会看到在这个电影上给大家展示的图景。我们的血液里面大量的是血红细胞,一毫升的血液里面有大概五十亿个血红细胞。
同时,我们还有大量的这种白细胞。而在癌症病人的血液里面一毫升血我们仅仅能够找到几个到几十个的循环肿瘤细胞。所以它们的数量是非常地稀少,从这几十亿个细胞里面去找寻这几个到几十个细胞,用大海捞针来形容一点都不过分。
假设我们有了很好的手段把它们准确地捕获下来,我们还遇到的困难就是对这几个细胞、几十个细胞,我们怎么去进行分析?我们现有的医学的手段,生物学的手段都是基于大量的细胞来进行的研究,对于这样的少量细胞,我们现有的技术无能为力。
单细胞测序技术,如何用于癌症治疗?
我们需要发展新的技术,而其中最为前沿的就是单细胞的测序技术。我们可以针对一个细胞,准确去获取它里面的基因组的信息,转录组的信息。那么把先进的单细胞的测序技术和循环肿瘤细胞这个关键的临床问题结合在一起,我们可以进行一个非常有创新性的研究。
首先,我们在医院里面把癌症病人的外周血进行抽取。我们的取血量大概是五毫升到十毫升之间,然后用这种单细胞的精确操纵和分离的办法,把癌症病人血液里面的循环肿瘤细胞准确地给分离出来。
然后,我们把这样一些细胞进行一个基因组的扩增。我们对标本的DNA的起始量要求要达到微克的量级,也就是10的负六次方。而我们从一个细胞里面能够分离出来的遗传物质只有皮克的量级,甚至更少。所以就有一个巨大的鸿沟。
就需要我们使用单细胞测序的技术去把这个微量的DNA准确地,高保真地把它扩增出来。当我们获得足够量的DNA的物质之后,我们就可以进行这种标准的基因测序,辅助于生物信息学的手段进行分析,我们就可以得到很多重要的临床信息。
在这里用一个案例来给大家演示,我们究竟从癌症病人的血液里面可以获取怎样重要的信息呢?这是一个典型的肺癌的患者。
他是一个原发癌发在肺部的患者,然后发生了一个肝部的转移。我们把这个病人外周血中的循环肿瘤细胞进行了准确地分离,进行了单细胞测序。在这里可以看到,我在这里列出来的是从单个循环肿瘤细胞里面获取的全基因组基因拷贝数变化的模式。
前面就看到红红蓝蓝的这样线,从第一个开始到最后,分别表示了我们人类的染色体。从一号染色体到二十二号染色体,然后是X、Y。我们可以看到最上面一行是一个正常的细胞。我们人类是一个二倍体,所以当我们的细胞没有发生变异的时候,我们是一个平整的在二的拷贝数的一个平整的信号。
那么我们看到下面的这些就是肿瘤的原发位、肿瘤的转移位,还有八个循环肿瘤细胞。我们看到它们上面有这种典型的基因组拷贝数的扩增和缺失。这是癌症的一个区别于正常细胞的一个典型的特征。正是因为有了这些基因的扩增和缺失,导致这个细胞获得了比正常细胞更加恶劣的生长能力,不受控制的生长能力,以及它能够获得更强的迁徙和转移的能力。
我们从血液里面获取了这个癌症病人循环肿瘤细胞的全基因组拷贝数模式,可以把它作为一个像ID一样,像一个指标一样去衡量这个病人的病情的分型。在这里可以看到,我们把不同的病人的癌症的循环肿瘤细胞的基因拷贝数变化模式放在一起去看,我们发现其中的这些病人存在了一定的相似性。这些病人都来自于肺癌的一个亚型,叫做肺腺癌。
我在上下分别展示了另外两个病人,他们来自于肺癌的另外一个亚型,叫做小细胞肺癌。我们可以看到中间的这一群细胞和上下两个细胞存在着明显的差别。这个分析就第一次证明了:通过循环肿瘤细胞的基因组拷贝数的分析,我们能够对癌症的这种亚型来进行一个鉴定和分离。
对于循环肿瘤细胞单细胞基因测序,不仅仅可以获取它的基因拷贝数变化模式,还可以获取这种和癌症发生发展重要的这些基因的点突变。
还要继续穿刺?癌症检测何时不再痛苦?
我们知道,我们一个人类的细胞大概有两万到三万个基因。这些基因在我们每天的生活发挥着非常重要的作用。一旦它们出现了问题,我们就会患上疾病。而对于癌症来说,我们有一些基因被称为癌基因,有一些基因被称为抑癌基因。
做一个简单的比喻,癌基因就好比一个油门,而抑癌基因就好比是一个刹车。只有当癌基因和抑癌基因都正常工作的情况下,我们身体的这辆汽车才能够平稳地行驶。而如果癌基因上发生了突变,它获得了异常的功能就好像油门失控一样,这辆车就会走向危险。如果抑癌基因发生了突变,发生了变化,就好像这个车的刹车出现了问题。同样也蕴含了巨大的危险和隐患。那么这癌基因的突变和抑癌基因的突变都是癌症发生了一个重要的指征。
这个病人来到医院的时候,首先他是一个肺腺癌,然后因为他的原位的肿瘤组织里面发现了有这个EGFR这样一个癌基因的一个突变,所以,医生给他制订了一个靶向的治疗,给他用了一个专门针对EGFR基因突变的药物。那么在药物治疗的过程中在一段时间之内,这个病人的病情得到了缓解。
在几个月之后,我们对他的血液进行了CTCs(循环肿瘤细胞)的分离和测序。我们就奇怪地发现这个血液里面不仅仅可以看到EGFR基因的突变,同时还看到了PIK3CA基因的突变,还有RB1、TB53这两个抑癌基因的失活。我们看到这个信息就非常地紧张。为什么呢?
因为PIK3CA基因的突变和这个肿瘤的耐药是直接相关系在一起,而RB1、TB53两个基因的失活和肿瘤从肺腺癌向小细胞肺癌的转化又直接地相关。于是我们把这个信息及时地反馈给了这个医生。我们的这个预测很不幸地就被证实了。这个病人不久之后就出现了药物的耐药,并且在他的肝部的转移位出现了向小细胞肺癌的转化。
信息的及时地、提前地这样一种预警可以为医生及时地改变治疗方案提供宝贵的时间。
那么我讲到现在,大家可能觉得我们用了一些很前沿的方法研究了一个很重要的问题。那么究竟和我们的实用和临床到底有什么样直接的关系?
为了把这个问题说清楚。首先我们要对现有的癌症检测的方法来作一个比较。如果有一个病人患了癌症去到肿瘤医院,那么现在的方法为了给他进行这种癌症的组织的鉴定和病理的分型用的办法一般叫做活检。
活检通俗地说叫穿刺。穿刺一般是在超声的引导之下,用一根针在这个病人的器官患病的部位,比如说如果是肺癌就是肺部,用一根针插进去,然后取一个很小的肿瘤标本出来,然后做病理学的鉴定。然后做一个基因的profiling,做一个基因突变的一个检测。这就是现在的方法。
但是这种方法具有的很大的一个隐患,就是首先第一个它的伤害性非常地大,不可能在疾病治疗的过程中反复地去使用。再者我们进行这样的深层器官的穿刺容易造成内出血,甚至人为的造成肿瘤的播散和转移。这就是当前我们使用活检存在的巨大的一个问题。
那么,如果我们能从血液里面来做像我们刚才演示的那样,从血液里面把这些肿瘤细胞分离出来,然后对它们进行基因测序。对它们进行病理诊断,极大地避免了当前活检所存在的这种巨大的危害。
那我们这里究竟能不能做到这样呢?我们在这个病例上也进行了一个研究。这样一个病人,我们在他疾病的治疗过程中,在化疗之前,在一线化疗之后,二线化疗之后,我们对他进行了循环肿瘤细胞的分离和测序。
我们可以看到,在疾病治疗的过程中。他的基因突变图谱确实存在着一个动态的变化。而准确地获取这些信息对于医生及时地去修改治疗方案有着非常宝贵的意义。就是来自血液里面的循环肿瘤细胞的基因测序和分析可以实现对于致癌的关键基因的准确的探测,并且通过基因拷贝数变化模式的这种鉴定可以为癌症的分型和预后提供重要的依据。
我们之前的这一部分的结果已经发表于这个国际著名的学术期刊——《美国国家科学院通讯》,也得到了各个科学杂志以及一些财经杂志的重点关注和报道。这是我们团队共同努力的一个结果。在此我特别感谢谢晓亮教授、王洁教授和张宁教授。
我们已经可以实现从肺癌到中国其它高发癌种的一个拓展性的研究。基于以循环肿瘤细胞作为媒介的一个癌症的血液检测,可以在我们的个体化医疗、精准医疗中发挥重要的作用。
基于血液的这种检测是一种伤害性非常小的检测方式。正因为它伤害性非常地小,所以我们可以在病人治疗的病程中可以反复地去使用,及时地跟踪他的病情的进展,或者说他有没有发生耐药的变化,从而可以帮助医生及时地去调整治疗的方案。癌症的血液检测能不能推广到我们日常的这种体检?
让我们在日常的体检中也去检测这些癌症的指标,然后来实现癌症的早诊早治呢?我想这是我们在未来五年之内科学家和我们这些医生一起要努力去实现的。
抗肿瘤药物,未来将实现个性化医疗
循环肿瘤细胞还有一个重要的功能就是我们不仅仅可以对它来进行基因测序,我们还可以把循环肿瘤细胞进行体外的一个培养。
我们不断地在讲精准的医疗、个体化的医疗,现阶段假设我们有十种抗肿瘤的药物,那这个十种抗肿瘤的药物去给病人使用的时候,我们的医生大部分的情况下是基于经验的判断,或者现阶段我们基于部分基因的基因测序的结果来进行使用,这算不算得上真正的个体化医疗呢?
我们如果能把循环肿瘤细胞从这个病人的血液里面准确地分离出来,然后在体外进行培养,把它培养成为一个系统的一个肿瘤细胞系,或者把它种植到免疫缺陷的老鼠身上构建一个人源的肿瘤老鼠模型,我们就可以在体外把这十种抗癌药物对这些细胞来分别来进行试用。
我们可以去看究竟哪一些药物能够更好地、有效地杀灭这个病人的肿瘤,以此来实现真正的针对每一个人的个性化医疗。
癌症病人的血液里面不仅仅只有循环肿瘤细胞能够作为癌症标志物,它还有肿瘤分泌出来的循环肿瘤DNA,还有肿瘤分泌出来的外泌体。如果我们能把这种血液里面的各种肿瘤标志物综合起来使用,可以极大地提升我们国家癌症早期预防和无创诊断的水平,能够造福广大的癌症患者。
虽然癌症很难治愈,很难被攻克,但是全世界的科学家和医学工作者都在不断地努力。我想伴随着我们现在基因技术的广泛应用,以及我们对于精准医疗的大力地推广,在不久的将来我们将会经历一个癌症从检测到治疗的一个重大的变革。
“特别声明:以上作品内容(包括在内的视频、图片或音频)为凤凰网旗下自媒体平台“大风号”用户上传并发布,本平台仅提供信息存储空间服务。
Notice: The content above (including the videos, pictures and audios if any) is uploaded and posted by the user of Dafeng Hao, which is a social media platform and merely provides information storage space services.”